АТОМ [французький atome, від латинського atomus, від грецького? Τομος (ουσ? Α) - неподільна (сутність)], частка речовини, найменша частина хімічного елемента, що є носієм його властивостей. Атоми кожного елемента індивідуальні за будовою і властивостями і позначаються хімічними символами елементів (наприклад, атом водню - Н, заліза - Fe, ртуті - Hg, урану - U і т. Д.). Атоми можуть існувати як у вільному стані, так і у зв'язаному (дивись Хімічний зв'язок). Все різноманіття речовин обумовлено різними поєднаннями атомів між собою. Властивості газоподібних, рідких і твердих речовин залежать від властивостей складових їх атомів. Всі фізичні і хімічні властивості атома визначаються його будовою і підкоряються квантовим законам. (Про історію розвитку вчення про атом дивись в статті Атомна фізика.)
Загальна характеристика будови атомів. Атом складається з важкого ядра, що володіє позитивним електричним зарядом, і оточуючих його легких електронів з негативними електричними зарядами, що утворюють електронні оболонки атома. Розміри атома визначаються розмірами його зовнішньої електронної оболонки і великі в порівнянні з розмірами ядра атома. Характерні порядки діаметрів, площ поперечного перерізу і обсягів атома і ядра складають:
Реклама
Атом 10-8 см 10-16 см2 10-24 см3
Ядро 10-12 см 10-24 см2 10-36 см3
Електронні оболонки атома не мають строго визначених кордонів, і значення розмірів атома в більшій або меншому ступені залежать від способів їх визначення.
Заряд ядра - основна характеристика атома, яка обумовлює його приналежність певного елемента. Заряд ядра завжди є цілим, кратним позитивного елементарного електричного заряду, рівного за абсолютним значенням заряду електрона -е. Заряд ядра дорівнює + Ze, де Z - порядковий номер (атомний номер). Z = 1, 2, 3, ... для атомів послідовних елементів в періодичній системі хімічних елементів, тобто для атомів Н, Не, Li, .... В нейтральному атомі ядро із зарядом + Ze утримує Z електронів із загальним зарядом - Ze. Атом може втратити або приєднати до електронів і стати позитивним або негативним іоном (к = 1, 2, 3, ... - кратність його іонізації). До атому певного елемента часто відносять і його іони. При написанні іони відрізняють від нейтрального атома індексом до + і до-; наприклад, О - нейтральний атом кисню, Про +, О2 +, О3 +, ..., О8 +, О, О2 - його позитивні і негативні іони. Сукупність нейтрального атома і іонів інших елементів з тим же числом електронів утворює ізоелектронними ряд, наприклад ряд водородоподобних атомів Н, Чи не +, Li2 +, Ве3 +, ....
Кратність заряду ядра атома елементарному заряду е отримала пояснення на підставі уявлень про будову ядра: Z дорівнює числу протонів в ядрі, заряд протона дорівнює + е. Маса атома зростає зі збільшенням Z. маса ядра атома приблизно пропорційна масовому числу А - загальному числу протонів і нейтронів в ядрі. Маса електрона (0,91 · 10-27 г) значно менше (приблизно в 1840 разів) маси протона або нейтрона (1,67? 10-24 г), тому маса атома в основному визначається масою його ядра.
Атоми даного елемента можуть відрізнятися масою ядра (число протонів Z постійно, число нейтронів А-Z може змінюватися); такі різновиди атомів одного і того ж елемента називаються ізотопами. Різниця маси ядра майже не позначається на будові електронних оболонок даного атома, що залежить від Z, і властивості атома. Найбільші відмінності у властивостях (ізотопні ефекти) виходять для ізотопів водню (Z = 1) через велику різницю в масах звичайного легкого атома водню (А = 1), дейтерію (А = 2) і тритію (А = 3).
Маса атома змінюється від 1,67? 10-24 г (для основного ізотопу атом водню, Z = 1, А = 1) до приблизно 4? 10-22 г (для атомів трансуранових елементів). Найбільш точні значення мас атомів можуть бути визначені методами мас-спектроскопії. Маса атома не дорівнює в точності сумі маси ядра і мас електронів, а трохи менше - на дефект маси ΔM = W / c2, де W - енергія освіти атома з ядра і електронів (енергія зв'язку), з - швидкість світла. Ця поправка порядку маси електрона me для важких атомів, а для легких нехтує мала (порядку 10-4 me).
Енергія атома і її квантування. Завдяки малим розмірам і великій масі атомне ядро можна приблизно вважати точковим і таким, що покоїться в центрі мас атома (загальний центр мас ядра і електронів знаходиться поблизу ядра, а швидкість руху ядра відносно центру мас атома мала в порівнянні зі швидкостями руху електронів). Відповідно атом можна розглядати як систему, в якій N електронів із зарядами - е рухаються навколо нерухомого притягає центру. Рух електронів в атомі відбувається в обмеженому обсязі, тобто є пов'язаною. повна внутрішня енергія атома Е дорівнює сумі кінетичних енергій Т всіх електронів і потенційної енергії U - енергії тяжіння їх ядром і відштовхування друг від друга.
Відповідно до теорії атома, запропонованої в 1913 році Нільсом Бором, в атомі водню один електрон із зарядом -е рухається навколо нерухомого центру з зарядом + е. Відповідно до класичної механікою кінетична енергія такого електрона дорівнює

де v - швидкість, p = mev - кількість руху (імпульс) електрона. Потенційна енергія (що зводиться до енергії кулонівського притягання електрона ядром) дорівнює

і залежить тільки від відстані r електрона від ядра. Графічно функція U (r) зображується кривої, необмежено спадної при зменшенні r, т. Е. При наближенні електрона до ядра. Значення U (r) при r → ∞ прийнято за нуль. При негативних значеннях повної енергії Е = Т + U <0 рух електрона є пов'язаною: воно обмежене в просторі значеннями r = rмaкc. При позитивних значеннях повної енергії Е = Т + U> 0 рух електрона є вільним - він може піти на нескінченність з енергією Е = Т = (1/2) mеv2, що відповідає іонізованному атому водню Н +. Таким чином, нейтральний атом водню - система електростатично пов'язаних ядра і електрона з енергією Е <0.
Повна внутрішня енергія атома Е - його основна характеристика як квантової системи (дивись Квантова механіка). Атом може тривалий час перебувати лише в станах з певною енергією - стаціонарних (незмінних в часі) станах. Внутрішня енергія квантової системи, що складається із зв'язаних мікрочасток (в тому числі атома), може приймати одне з дискретного (переривчастого) ряду значень

Кожному з цих «дозволених» значень енергії відповідає одне або кілька стаціонарних квантових станів. Проміжними значеннями енергії (наприклад, лежать між Е1 і Е2, Е2 і Е3, і т.д.) система володіти не може, про таку систему говорять, що її енергія квантована. Будь-яка зміна Е пов'язано з квантовим (стрибкоподібним) переходом системи з одного стаціонарного квантового стану в інше (дивись нижче).
Можливі дискретні значення (3) енергії атома графічно можна зобразити за аналогією з потенційною енергією тіла, піднятого на різні висоти (на різні рівні), у вигляді схеми рівнів енергії, де кожному значенню енергії відповідає пряма, проведена на висоті Ei, i = 1, 2, 3, ... (рис. 1). Найнижчий рівень E1, відповідний найменшій можливій енергії атома, називається основним, а всі інші (Ei> E1), i = 2, 3, 4, ...) - збудженими, т. К. Для переходу на них (переходу до відповідних стаціонарні збуджені стани з основного) необхідно порушити систему - повідомити їй ззовні енергію Ei-E1.
 Квантування енергії атома є наслідком хвильових властивостей електронів. Відповідно до принципу корпускулярно-хвильового дуалізму, руху мікрочастинки маси m із швидкістю v відповідає довжина хвилі λ = h / mv, де h - постійна Планка. Для електрона в атомі λ порядку 10-8см, тобто близько лінійних розмірів атома, і облік хвильових властивостей електрона в атомі є необхідним. Пов'язане рух електрона в атомі схоже зі стоячою хвилею, і його слід розглядати не як рух матеріальної точки по траєкторії, а як складний хвильовий процес. Для стоячої хвилі в обмеженому обсязі можливі лише певних значень довжини хвилі λ (і, отже, частоти коливань v). Згідно з квантовою механікою, енергія атома Е пов'язана з v співвідношенням Е = hν і тому може приймати лише певні значення. Вільне, необмежене в просторі поступальний рух мікрочастинки, наприклад рух електрона, відірваного від атома (з енергією Е> 0), схоже з поширенням хвилі, що біжить в необмеженій обсязі, для якої можливі будь-які значення λ (і v). Енергія такої вільної мікрочастинки може приймати будь-які значення (НЕ квантів, має безперервний енергетичний спектр). Така безперервна послідовність відповідає іонізованному атому. Значення Е∞ = 0 відповідає кордоні іонізації; різницю Е∞-Е1 = Еіон називається енергією іонізації (дивись в статті іонізації потенціал); для атома водню вона дорівнює 13,6 еВ.
Квантування енергії атома є наслідком хвильових властивостей електронів. Відповідно до принципу корпускулярно-хвильового дуалізму, руху мікрочастинки маси m із швидкістю v відповідає довжина хвилі λ = h / mv, де h - постійна Планка. Для електрона в атомі λ порядку 10-8см, тобто близько лінійних розмірів атома, і облік хвильових властивостей електрона в атомі є необхідним. Пов'язане рух електрона в атомі схоже зі стоячою хвилею, і його слід розглядати не як рух матеріальної точки по траєкторії, а як складний хвильовий процес. Для стоячої хвилі в обмеженому обсязі можливі лише певних значень довжини хвилі λ (і, отже, частоти коливань v). Згідно з квантовою механікою, енергія атома Е пов'язана з v співвідношенням Е = hν і тому може приймати лише певні значення. Вільне, необмежене в просторі поступальний рух мікрочастинки, наприклад рух електрона, відірваного від атома (з енергією Е> 0), схоже з поширенням хвилі, що біжить в необмеженій обсязі, для якої можливі будь-які значення λ (і v). Енергія такої вільної мікрочастинки може приймати будь-які значення (НЕ квантів, має безперервний енергетичний спектр). Така безперервна послідовність відповідає іонізованному атому. Значення Е∞ = 0 відповідає кордоні іонізації; різницю Е∞-Е1 = Еіон називається енергією іонізації (дивись в статті іонізації потенціал); для атома водню вона дорівнює 13,6 еВ.
Розподіл електронної щільності. Точне положення електрона в атомі в даний момент часу встановити не можна внаслідок невизначеностей співвідношення. Стан електрона в атомі визначається його хвильової функцією, певним чином залежить від його координат; квадрат модуля хвильової функції характеризує щільність ймовірності знаходження електрона в даній точці простору. Хвильова функція в явному вигляді є рішенням Шредінгера рівняння.
Таким чином, стан електрона в атомі можна характеризувати розподілом в просторі його електричного заряду з деякою щільністю - розподілом електронної щільності. Електрони як би «розмазані» в просторі і утворюють «електронну хмару». Така модель правильніше характеризує електрони в атомі, ніж модель точкового електрона, що рухається по строго визначених орбітах (в теорії атома Бора). Разом з тим кожній такій боровськой орбіті можна зіставити конкретний розподіл електронної щільності. Для основного рівня енергії E1 електронна щільність концентрується поблизу ядра; для збуджених рівнів енергії Е2, Е3, Е4 ... вона розподіляється на все більших середніх відстанях від ядра. У багатоелектронних атомі електрони групуються в оболонки, що оточують ядро на різних відстанях і характеризуються певними розподілами електронної щільності. Міцність зв'язку електронів з ядром в зовнішніх оболонках менше, ніж у внутрішніх, і слабкіше за все електрони пов'язані в самій зовнішній оболонці, що володіє найбільшими розмірами.
Облік спина електрона і спина ядра. В теорії атома дуже істотний облік спина електрона - його власного (спину) моменту кількості руху, з наочної точки зору відповідного обертанню електрона навколо власної осі (якщо електрон розглядати як частку малих розмірів). Зі спіном електрона пов'язаний сто власний (спіновий) магнітний момент. Тому в атомі необхідно враховувати, поряд з електростатичними взаємодіями, і магнітні взаємодії, які визначаються спінові магнітним моментом і орбітальним магнітним моментом, пов'язаним з рухом електрона навколо ядра; магнітні взаємодії малі в порівнянні з електростатичними. Найбільш істотний вплив спина в багатоелектронних атомах: від спина електронів залежить заповнення електронних оболонок атома певним числом електронів.
Ядро в атомі також може володіти власним механічним моментом - ядерним спіном, з яким пов'язаний ядерний магнітний момент в сотні і тисячі разів менший електронного. Існування спинив призводить до додаткових, дуже малим взаємодіям ядра і електронів (дивись нижче).
Квантові стану атома водню. Найважливішу роль в квантової теорії атома грає теорія простого одноелектронного атома, що складається з ядра з зарядом + Ze і електрона із зарядом е, тобто теорія атома водню Н і водородоподобних іонів Чи не +, Li2 +, Ве3 +, ..., звана зазвичай теорією атома водню. Методами квантової механіки можна отримати точну і повну характеристику станів електрона в одноелектронному атомі. Завдання про Багатоелектронні атомі вирішується лише приблизно; при цьому виходять з результатів рішення задачі про одноелектронному атомі.
Енергія одноелектронного атома в нерелятивістському наближенні (без урахування спина електрона) дорівнює

ціле число n = 1, 2, 3, ... визначає можливі дискретні значення енергії - рівні енергії - і називається головним квантовим числом, R - постійна Рідберга, рівна 13,6 еВ. Рівні енергії атома сходяться (згущуються) до кордону іонізації Е∞ = 0, що відповідає n = ∞. Для водородоподобних іонів змінюється (в Z2 раз) лише масштаб значень енергій. Енергія іонізації водородоподобного атома (енергія зв'язку електрона) дорівнює (в еВ)

що дає для Н, Чи не +, Li2 +, ... значення 13,6еВ, 54,4 еВ, 122,4 еВ, ....
Основна формула (4) відповідає виразу U (r) = -Ze2 / r для потенційної енергії електрона в електричному полі ядра з зарядом + Ze. Ця формула була вперше виведена Н. Бором шляхом розгляду руху електрона навколо ядра по круговій орбіті радіуса r і є точним рішенням рівняння Шредінгера для такої системи. Рівнями енергії (4) відповідають орбіти радіуса

де постійна а0 = 0,529 · 10-8 см = = 0,529 А - радіус першої кругової орбіти атома водню, що відповідає її основному рівню (цим боровським радіусом часто користуються в якості зручною одиниці для вимірювань довжин в атомній фізиці). Радіус орбіт пропорційний квадрату головного квантового числа n2 і обернено пропорційний Z; для водородоподобних іонів масштаб лінійних розмірів зменшується в Z раз в порівнянні з атомом водню. Релятивістське опис атома водню з урахуванням спина електрона дається Дирака рівнянням.
Згідно з квантовою механікою, стан атома водню повністю визначається дискретними значеннями чотирьох фізичних величин: енергії Е; орбітального моменту МL (моменту кількості руху електрона щодо ядра); проекції Мlz орбітального моменту на довільно обраний напрям z; проекції Msz спинового моменту (власного моменту кількості руху електрона Ms). Можливі значення цих фізичних величин, в свою чергу, визначаються квантовими числами n, l, ml, ms відповідно. У наближенні, коли енергія атома водню описується формулою (4), вона визначається лише головним квантовим числом n, що приймає цілочисельні значення 1, 2, 3, .... Рівню енергії із заданим n відповідає кілька станів, що розрізняються значеннями орбітального (азимутального) квантового числа l = 0, 1, ..., n-1. Стану з заданими значеннями n і l прийнято позначати як 1s, 2s, 2р, 3s, ..., де цифри вказують значення n, а букви s, р, d, f (далі за латинським алфавітом) - відповідно значення l = 0, 1, 2, 3. При заданих n і l число різних станів дорівнює 2 (2l + 1) - числу комбінацій значень магнітного орбітального квантового числа ml магнітного спінового числа ms (перше приймає 2l + 1 значень, друге - 2 значення). Загальна кількість різних станів із заданими n і l виходить рівним 2n2. Таким чином, кожному рівню енергії атома водню відповідає 2,8, 18, ... 2n2 (при n = 1, 2, 3, ...) різних стаціонарних квантових станів. Якщо рівнем енергії відповідає лише одне квантовий стан, то його називають невиродженим, якщо два або більше - виродженим (дивись Виродження в квантової теорії), а число таких станів g називається ступенем або кратністю виродження (для невироджених рівнів енергії g = 1). Рівні енергії атома водню є виродженими, а їх ступінь виродження gn = 2n2.
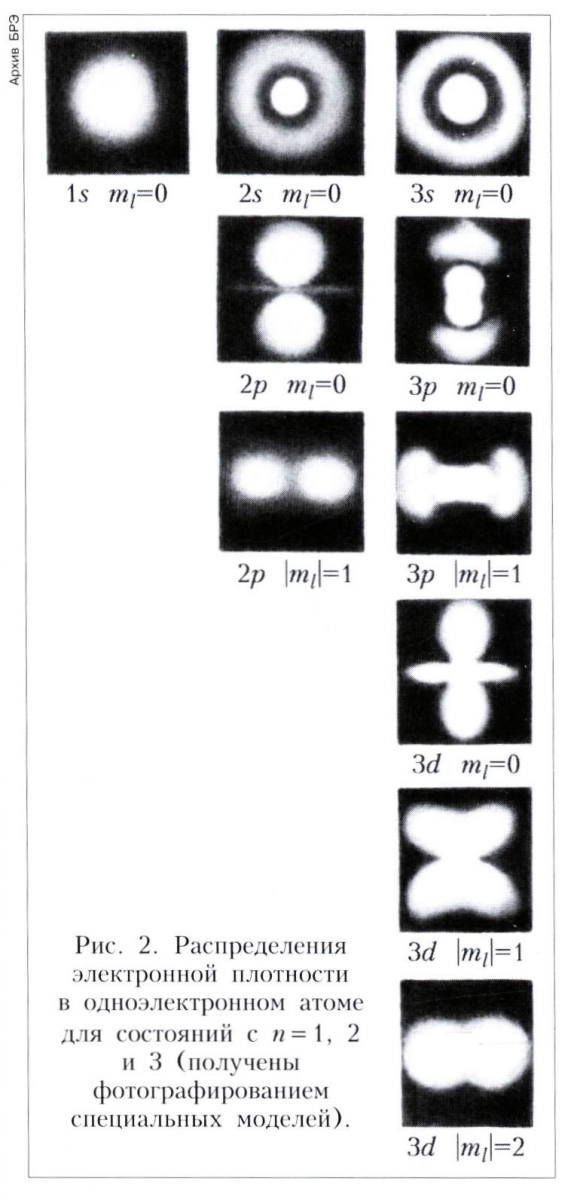
Для різних станів атома водню виходить і різний розподіл електронної щільності. Воно залежить від квантових чисел n, l і [ml] При цьому електронна щільність для s-станів (l = 0) відмінна від нуля в центрі, т. Е. В місці знаходження ядра, і не залежить від напрямку (сферично симетрична), а для інших станів (l> 0) вона дорівнює нулю в центрі і залежить від напрямку. Розподіл електронної щільності для станів атома водню з n = 1, 2, 3 показано на малюнку 2; розміри «електронної хмари» зростають відповідно до формули (6) пропорційно n2 (масштаб на малюнку 2 зменшується при переході від n = 1 до n = 2 і від n = 2 до n = 3). Квантові стану електрона в водородоподобних іони характеризуються тими ж чотирма квантовими числами n, l, ml і ms, що і в атомі водню. Зберігається і розподіл електронної щільності, тільки вона збільшується в Z раз.
 Дія на атом зовнішніх полів. Атом як електрична система в зовнішньому електричному і магнітному полях набуває додаткову енергію. Електричне поле поляризує атом - зміщує електронні хмари щодо ядра (дивись Поляризуемость атомів, іонів і молекул), а магнітне поле орієнтує певним чином магнітний момент атома, пов'язаний з рухом електрона навколо ядра (з орбітальним моментом Ml) і його спіном. Різним станам атома водню з тією ж енергією Еn в зовнішньому полі відповідають різні значення додаткової енергії ДЕ, і вироджених рівень енергії En розщеплюється на ряд підрівнів. Як розщеплення рівнів енергії в електричному полі - Штapкa ефект, - так і їх розщеплення в магнітному полі - Зеемана ефект - пропорційні напруженості відповідних полів.
Дія на атом зовнішніх полів. Атом як електрична система в зовнішньому електричному і магнітному полях набуває додаткову енергію. Електричне поле поляризує атом - зміщує електронні хмари щодо ядра (дивись Поляризуемость атомів, іонів і молекул), а магнітне поле орієнтує певним чином магнітний момент атома, пов'язаний з рухом електрона навколо ядра (з орбітальним моментом Ml) і його спіном. Різним станам атома водню з тією ж енергією Еn в зовнішньому полі відповідають різні значення додаткової енергії ДЕ, і вироджених рівень енергії En розщеплюється на ряд підрівнів. Як розщеплення рівнів енергії в електричному полі - Штapкa ефект, - так і їх розщеплення в магнітному полі - Зеемана ефект - пропорційні напруженості відповідних полів.
До розщеплювання рівнів енергії приводять і малі магнітні взаємодії всередині атома. Для атома водню і водородоподобних іонів має місце спін-орбітальна взаємодія - взаємодія спинового і орбітального моментів електрона; воно обумовлює так звану тонку структуру рівнів енергії - розщеплення збуджених рівнів En (при n> 1) на підрівні. Для всіх рівнів енергії атома водню спостерігається і надтонка структура, обумовлена дуже малими магнітними взаємодіями ядерного спина з електронними моментами.
Електронні оболонки багатоелектронних атомів. Теорія атома, що містять 2 або більше електронів, принципово відрізняється від теорії атома водню, так як в такому атомі є взаємодіють один з одним однакові частки - електрони. Взаємне відштовхування електронів в багатоелектронних атомі істотно зменшує міцність їх зв'язку з ядром. Наприклад, енергія відриву єдиного електрона в іоні гелію (Не +) дорівнює 54,4 еВ, в нейтральному ж атомі гелію в результаті відштовхування електронів енергія відриву одного з них зменшується до 24,6 еВ. Для зовнішніх електронів більш важких атомів зменшення міцності їх зв'язку через відштовхування внутрішніми електронами ще значніше. Важливу роль в багатоелектронних атомах грають властивості електронів як однакових мікрочастинок (дивись Тотожності принцип), що володіють спіном s = 1/2, для яких справедливий Паулі принцип. Згідно з цим принципом, в системі електронів не може бути більше одного електрона в кожному квантовому стані, що призводить до утворення електронних оболонок атома, що заповнюються строго певними числами електронів.
З огляду на непомітність взаємодіючих між собою електронів, має сенс говорити тільки про квантових станах атома в цілому. Однак приблизно можна розглядати квантові стану окремих електронів і характеризувати кожен з них сукупністю квантових чисел n, l, ml і ms, аналогічно електрону в атомі водню. При цьому енергія електрона виявляється залежною не тільки від n, як в атомі водню, але і від l; від ml і ms вона як і раніше не залежить. Електрони з даними n і l в багатоелектронних атомі мають однакову енергію і утворюють певну електронну оболонку. Такі еквівалентні електрони і утворені ними оболонки позначають, як і квантові стану і рівні енергії з заданими n і l, символами ns, nр, nd, nf, ... (для 1 = 0, 1, 2,3, ...) і говорять про 2р-електронах, 3s-о6олочках і т.п.
Згідно з принципом Паулі, будь-які 2 електрона в атомі повинні знаходитися в різних квантових станах і, отже, відрізнятися хоча б одним з чотирьох квантових чисел n, l, ml і ms, а для еквівалентних електронів (n і l однакові) - значеннями ml і ms . Число пар ml, ms, т. Е. Число різних квантових станів електрона з заданими n і l, і є ступінь виродження його рівня енергії gl = 2 (2l + 1) = 2, 6, 10, 14, .... Воно визначає число електронів в повністю заповнених електронних оболонках. Таким чином, s-, р-, d-, f-, ... оболонки заповнюються 2, 6, 10, 14, ... електронами, незалежно від значення n. Електрони з даними n утворюють шар, що складається з оболонок з l = 0, 1, 2, ..., n - 1 і заповнюється 2n2 електронами, так званий К-, L-, М, N-шар. При повному заповненні маємо:

У кожному шарі оболонки з меншими l характеризуються більшою електронною щільністю. Міцність зв'язку електрона з ядром зменшується зі збільшенням n, а при заданому n - зі збільшенням l. Чим слабкіше пов'язаний електрон у відповідній оболонці, тим вище лежить його рівень енергії. Ядро з заданим Z приєднує електрони в порядку зменшення міцності їх зв'язку: спочатку два електрона 1s, потім два електрона 2s, шість електронів 2р і т. Д. Атому кожного хімічного елемента притаманне певне розподіл електронів по оболонок - його електронна конфігурація, наприклад:

(Число електронів в даній оболонці вказується індексом справа зверху). Періодичність у властивостях елементів визначається схожістю зовнішніх електронних оболонок атома. Наприклад, нейтральні атоми Р, As, Sb, Bi (Z = 15, 33, 51, 83) мають по три р-електрона у зовнішній електронній оболонці, подібно атому N, і схожі з ним за хімічними та багатьом фізичним властивостям.
Кожен атом характеризується нормальною електронною конфігурацією, що виходить, коли всі електрони в атомі зв'язуються найміцніший, і збудженими електронними конфігураціями, коли один або кілька електронів пов'язані слабше - знаходяться на більш високих рівнях енергії. Наприклад, для атома гелію поряд з нормальною 1s2 можливі збуджені електронні конфігурації: 1s2s, 1s2р, ... (збуджений один електрон), 2s2, 2s2р, ... (порушені обидва електрона). Певної електронної конфігурації відповідає один рівень енергії атома в цілому, якщо електронні оболонки цілком заповнені (наприклад, нормальна конфігурація атома Ne 1s22s22р6), і ряд рівнів енергії, якщо є частково заповнені оболонки (наприклад, нормальна конфігурація атома азоту 1s22s22р3 для якої оболонка 2р заповнена наполовину ). При наявності частково заповнених d- і f-оболонок число рівнів енергії, відповідних кожної конфігурації, може досягати багатьох сотень, так що схема рівнів енергії атома з частково заповненими оболонками виходить дуже складною. Основним рівнем енергії атома є найнижчий рівень нормальної електронної конфігурації.
Квантові переходи в атомі. При квантових переходах атом переходить з одного стаціонарного стану в інший - з одного рівня енергії на інший. При переході з більш високого рівня енергії Ei на більш низький Ек атом віддає енергію Ei - Ek, при зворотному переході отримує її. Як для будь-якої квантової системи, для атома квантові переходи можуть бути двох типів: з випромінюванням (оптичні переходи) і без випромінювання (Безвипромінювальні, або неоптичні, переходи). Найважливіша характеристика квантового переходу - його ймовірність, що визначає, як часто цей перехід може відбуватися.
При квантових переходах з випромінюванням атом поглинає (перехід Ек → Ei) або випускає (перехід Ei → Ек) електромагнітне випромінювання. Електромагнітна енергія поглинається і випромінюється атомом у вигляді кванта світла - фотона, - що характеризується певною частотою коливань v, згідно співвідношенню:

де hv - енергія фотона. Співвідношення (7) являє собою закон збереження енергії для мікроскопічних процесів, пов'язаних з випромінюванням.
Атом в основному стані може тільки поглинати фотони, а в збуджених станах може, як поглинати, так і випускати їх. Вільний атом в основному стані може існувати необмежено довго. Тривалість перебування атома в збудженому стані (час життя цього стану) обмежена, атом спонтанно (мимовільно), частково або повністю втрачає енергію збудження, випускаючи фотон і переходячи на більш низький рівень енергії; поряд з таким спонтанним випусканням можливо і вимушене випускання, що відбувається, подібно поглинання, під дією фотонів тієї ж частоти. Час життя збудженого атома тим менше, чим більша ймовірність спонтанного переходу, для атома водню воно порядку 10-8 с.
Сукупність частот v можливих переходів з випромінюванням визначає атомний спектр відповідного атома: сукупність частот переходів з нижніх рівнів на верхні - його спектр поглинання, сукупність частот переходів з верхніх рівнів на нижні - спектр випускання. Кожному такому переходу в атомному спектрі відповідає певна спектральна лінія частоти v.
При безвипромінювальних квантових переходах атом отримує або віддає енергію при взаємодії з іншими частинками, з якими він стикається в газі або тривалий час пов'язаний в молекулі, рідини або твердому тілі. У газі атом можна вважати вільним у проміжках часу між зіткненнями; під час зіткнення (удару) атом може перейти на більш низький або високий рівень енергії. Таке зіткнення називається непружним (на противагу пружного зіткнення, при якому змінюється тільки кінетична енергія поступального руху атома, а його внутрішня енергія залишається незмінною). Важливий окремий випадок - зіткнення вільного атома з електроном; зазвичай електрон рухається швидше атома, час зіткнення дуже мало і можна говорити про електронний ударі. Порушення атома електронним ударом є одним з методів визначення його рівнів енергії.
Хімічні та фізичні властивості атома. Більшість властивостей атома визначається будовою і характеристиками його зовнішніх електронних оболонок, в яких електрони пов'язані з ядром порівняно слабо (енергії зв'язку від декількох еВ до декількох десятків еВ). Будова внутрішніх оболонок атома, електрони яких пов'язані набагато міцніше (енергії зв'язку в сотні, тисячі і десятки тисяч еВ), проявляється лише при взаємодіях атома з швидкими частинками і фотонами високих енергій (більше сотень еВ). Такі взаємодії визначають рентгенівські спектри атома і розсіювання швидких частинок (дивись Дифракція часток). Від маси атома залежать його механічні властивості при русі атома як цілого - кількість руху, кінетична енергія. Від механічних і пов'язаних з ними магнітних і електричних моментів атома залежать різні резонансні та інші фізичні властивості атома (дивись Електронний парамагнітний резонанс, Ядерний магнітний резонанс, Ядерний квадрупольний резонанс).
Електрони зовнішніх оболонок атома легко піддаються зовнішнім впливам. При зближенні атомів виникають сильні електростатичні взаємодії, які можуть призводити до утворення хімічного зв'язку. Більш слабкі електростатичні взаємодії двох атомів виявляються в їх взаємної поляризації - зміщення електронів щодо ядер, найбільш сильному для слабо пов'язаних зовнішніх електронів. Виникають поляризаційні сили тяжіння між атомами, які треба враховувати вже на великих відстанях між ними. Поляризація атома відбувається і в зовнішніх електричних полях; в результаті рівні енергії атома зміщуються і, що особливо важливо, вироджені рівні енергії розщеплюються (ефект Штарка). Поляризація атома може виникнути під дією електричного поля світлової (електромагнітної) хвилі; вона залежить від частоти світла, що обумовлює залежність від неї і показника заломлення (дивись Дисперсія світла), пов'язаного з поляризуемостью атома. Тісний зв'язок оптичних характеристик атома з його електричними властивостями особливо яскраво проявляється в його оптичних спектрах.
Магнітні властивості атомів визначаються в основному будовою їх електронних оболонок. Магнітний момент атома залежить від його механічного моменту (дивись Магнітомеханічне відношення), в атомі з повністю заповненими електронними оболонками він дорівнює нулю, так само, як і механічний момент. Атоми з частково заповненими зовнішніми електронними оболонками мають, як правило, відмінними від нуля магнітними моментами і є парамагнітним. У зовнішньому магнітному полі всі рівні атомів, у яких магнітний момент не дорівнює нулю, розщеплюються - має місце ефект Зеемана. Всі атоми мають діамагнетизмом, який обумовлений виникненням у них магнітного моменту під дією зовнішнього магнітного поля (так званого індукованого магнітного моменту, аналогічного електричному дипольному моменту атома).
При послідовної іонізації атома, тобто при відриві його електронів, починаючи з самих зовнішніх в порядку збільшення міцності їх зв'язку, відповідно змінюються всі властивості атома, які визначаються його зовнішньою оболонкою. Зовнішніми стають все більш міцно пов'язані електрони; в результаті сильно зменшується здатність атома поляризуватися в електричному полі, збільшуються відстані між рівнями енергії і частоти оптичних переходів між цими рівнями (що призводить до зміщення спектрів в сторону все більш коротких довжин хвиль). Ряд властивостей виявляє періодичність: подібними виявляються властивості іонів з аналогічними зовнішніми електронами; наприклад, N3 + (два електрона 2s) виявляють схожість з N5 + (два електрона 1s). Це відноситься до характеристик і відносного розташуванню рівнів енергії і до оптичних спектрах, до магнітних моментів атома і так далі. Найбільш різка зміна властивостей відбувається при видаленні останнього електрона з зовнішньої оболонки, коли залишаються лише повністю заповнені оболонки, наприклад при переході від N4 + до N5 + (електронні конфігурації 1s22s і 1s2). В цьому випадку іон найбільш стійкий і його повний механічний і повний магнітний моменти дорівнюють нулю.
Властивості атома, що знаходиться в зв'язаному стані (наприклад, що входить до складу молекули), відрізняються від властивостей вільного атома. Найбільші зміни зазнають властивості атома, які визначаються самими зовнішніми електронами, які беруть участь у приєднанні даного атома до іншого. Разом з тим властивості, які визначаються електронами внутрішніх оболонок, можуть практично не зміниться, як це має місце для рентгенівських спектрів. Деякі властивості атома можуть відчувати порівняно невеликі зміни, за якими можна отримати інформацію про характер взаємодій пов'язаних атомів. Важливим прикладом може служити розщеплення рівнів енергії атома в кристалах і комплексних з'єднаннях, яке відбувається під дією електричних полів, створюваних оточуючими іонами.
Експериментальні методи дослідження структури атома, його рівнів енергії, його взаємодій з іншими атомами, елементарними частинками, молекулами, зовнішніми полями і так далі різноманітні, однак основна інформація міститься в його спектрах. Методи атомної спектроскопії у всіх діапазонах довжин хвиль, і особливо методи сучасної лазерної спектроскопії, дозволяють вивчати все більш тонкі ефекти, пов'язані з атомом. З початку 19 століття існування атома для вчених було очевидним, однак експеримент по доведенню реальності його існування було поставлено Ж. Перреном на початку 20 століття. З розвитком мікроскопії з'явилася можливість отримувати зображення атомів на поверхні твердих тіл. Вперше атом побачив Е. Мюллер (США, 1955) за допомогою винайденого їм автоіонного мікроскопа. Сучасні атомно-силові та тунельні мікроскопи дозволяють отримувати зображення поверхонь твердих тіл з хорошим дозволом на атомному рівні (дивись малюнок 3).

Мал. 3. Зображення атомної структури поверхні кремнію, отримане професором Оксфордського університету М. Капстеллом за допомогою скануючого тунельного мікроскопа.
Існують і широко використовуються в різних дослідженнях так звані екзотичні атоми, наприклад мюонні атоми, т. Е. Атоми, в яких всі або частину електронів замінені негативними мюонами, мюони, позитроній, а також адронні атоми, що складаються із заряджених піонів, каонов, протонів, дейтронів та інших. Здійснено також перші спостереження атома антиводню (2002) - атома, що складається з позитрона і антипротона.
Літ .: Борн М. Атомна фізика. 3-е изд. М., 1970; Фано У., Фано Л. Фізика атомів і молекул. М., 1980; Шпольський Е. В. Атомна фізика. 7-е изд. М., 1984. Т. 1-2; Ельяшевич М. А. Атомна і молекулярна спектроскопія. 2-е изд. М., 2000. ..
М. А. Ельяшевич.
Ουσ?Маса атома змінюється від 1,67?
Г (для основного ізотопу атом водню, Z = 1, А = 1) до приблизно 4?




